一叶知秋,见微知著
当组织器官发生损伤或病变时
细胞死亡释放的染色质片段就会进入体循环
携带着可追溯来源的“身份印记”
仅靠一滴血
能否识别病变来源组织及潜在受累器官?
北大团队及合作者提出了
一种新的表观液体活检方法
在结直肠癌、冠心病和淋巴瘤等
真实患者队列中
这项技术显示出较强的病变溯源、早期发现
分型和预后评估潜力
距离常规临床应用
仍需更大规模临床验证与产业化推进
未来,团队将开展覆盖数十种高发疾病的
多中心前瞻性研究
重点突破胰腺癌、脑部肿瘤、前列腺癌
及神经系统疾病的临床亟需场景
为精准医疗探索更多可能
2026年3月4日,北京大学未来技术学院、北京大学-清华大学生命科学联合中心何爱彬团队,联合北京大学第三医院血液内科景红梅团队及合作者在国际权威期刊Nature(《自然》)上,在线发表了题为“Cell-free chromatin state tracing reveals disease origin and therapy responses”(游离DNA染色质状态检测技术揭示疾病起源与治疗应答)的文章。
该研究开发了具有自主知识产权的新一代表观液体活检技术cf-EpiTracing,通过检测血浆中游离染色质的多组蛋白修饰信息,结合机器学习算法,在多病种真实患者队列中显示出无创识别病变来源组织、发现早期病变并评估预后的潜力,为液体活检临床转化提供了新方向。

《游离DNA染色质状态检测技术揭示疾病起源与治疗应答》一文发表于Nature

何爱彬

景红梅
从“细胞密码”到“血液指纹”——理念传承,开启液体活检新范式
就在一年前(2025年2月),何爱彬团队在Nature发表成果,开发了全基因组覆盖度单细胞多模态组蛋白修饰检测方法,重建胚胎发育过程中染色质状态刻画的细胞命运动态演化图谱,首次实现以表观编码对细胞谱系分化实现可追踪、可溯源的解析和驱动转录因子鉴定。这项成果为理解生命起源提供了新视角,填补了国际上发育生物学领域的理论空白,也为临床医学、癌症治疗等多个领域提供了全新的研究工具和理论支持。

《胚胎谱系追踪的基因组覆盖单细胞组蛋白修饰》一文发表于Nature
一个大胆的设想随之而来:如果细胞内的“密码”能决定它的命运,那么当细胞死亡后,释放到血液中的染色质碎片,是否还保留着来源组织器官的“身份印记”?理论上,只要我们能读懂这些碎片上的多模态表观遗传信息,就能反向推导出它们来自哪个器官,从而精准定位病灶。
然而,血浆分子背景高度复杂,疾病相关的调控信号常被大量生理噪声所掩盖。现有液体活检多聚焦基因突变、单一表观标志物或游离RNA,难以稳定、精准地刻画疾病全貌,更无法实现高分辨率的组织器官溯源。
如何在极低丰度且高度混杂的血浆样本中,系统重构染色质调控图谱,建立可用于疾病精准溯源的表观“身份指纹”? 这正是何爱彬团队在2025年的研究之上,向临床应用发起的全新攻关。
在2026年3月4日发表于Nature的工作中,团队及合作者开发了具有自主知识产权的新一代表观液体活检技术cf-EpiTracing,通过机器学习整合血浆游离染色质上的多模态组蛋白修饰编码调控元件信息,在真实患者队列中显示出识别病变来源组织、发现早期病变、辅助分型与预后评估的潜力。该成果标志着液体活检从以“基因检测”为主,迈向不依赖基因表达,以 “染色质解析”为视角的全身组织器官无偏诊断新阶段。
给一滴血里的信息,重新装上“解码器”——技术赋能,实现血浆多模态整合解析
传统液体活检技术多依赖有限检测维度。这类策略依赖已知标志物,不仅难以在高度异质和低丰度背景下实现稳定检测,也缺乏对组织来源进行精确判定的能力。在表观组学层面,既往方法多聚焦于DNA修饰(如5mC、5hmC)或转录组层面。这本质上是一种以功能终点为导向的局部解析模式,就像是只盯着功能终点看,而难以在复杂的血液环境中捕捉微弱信号,更无法精准定位病灶源头。这种局部解析模式,缺乏对细胞身份的全局把控。
针对这一关键瓶颈,研究者构建了基于自动化平台的cf-EpiTracing技术体系,实现了血浆中多种组蛋白修饰标记的同步富集与多模态整合解析。该方法突破了传统检测“预设标志物”的思路限制,以多模态表观调控为中心,以全局视角对组织器官进行了无偏溯源与健康状况评估。
在技术性能上,通过流程优化与建库策略创新,该方法可在低至25μL血浆中实现检测,但更大样本体积(50–200μL)表现更稳健。在信噪比、有效读段数、操作简易程度等方面均显著优于既有技术,为进一步临床转化提供了基础。
在数据分析层面,研究者也一改旧辙。不同于以往依赖转录组的间接推测,cf-EpiTracing引入ChromHMM分析框架,将复杂的表观特征整合成一套名为 ICSs 的通用语言。这就像将难懂的调控信号翻译成了清晰的“表观遗传图谱”,使得组织器官的来源精准可辨。基于此,团队已成功构建起覆盖肿瘤、心血管等多种疾病的大规模血浆表观图谱。
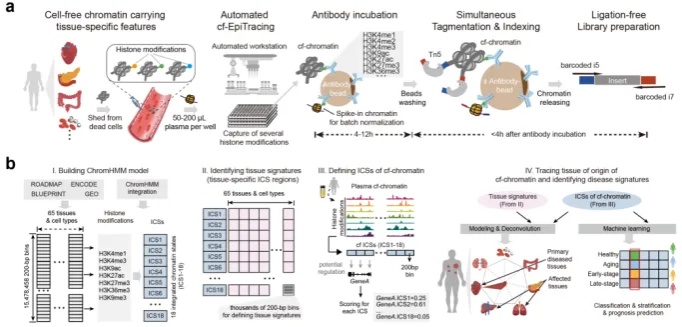
实验技术流程图与多模态整合溯源分析流程图
给全身器官,都建一份“健康档案”——范式创新,推动无创诊断迈向更高水平
依托多模态血浆游离染色质状态整合构建的“表观遗传图谱”,cf-EpiTracing实现了对全身多组织来源信号的精准定量。这意味着,仅需一次血浆检测,研究者便可同步锁定主要病变组织、排查潜在受累器官,并洞察系统性改变。
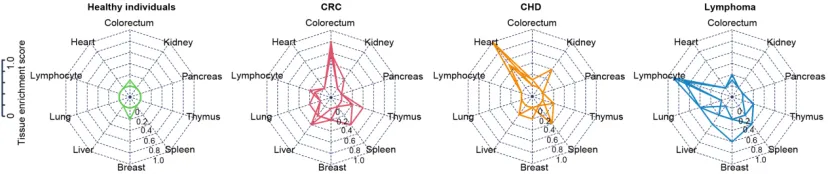
无偏诊断患病器官与受累器官
为实现真正的“无偏溯源”,研究团队构建了以健康人群为参照的组织富集评分模型。这相当于为每个器官设立了“标准基线”,从而无需依赖临床先验信息,便能敏锐识别出异常的组织信号。基于此,不同疾病分别呈现出了独特信号:冠心病以心脏信号显著升高为特征,结直肠癌突出结直肠来源信号,淋巴瘤则以淋巴细胞信号为主,体现出跨疾病精准溯源能力。更具临床突破性的是,在某些影像学尚未检出异常的阶段,该模型已具有能力提前捕捉潜在受累器官的求救信号。例如,在结直肠癌患者中发现肝脏信号升高,在淋巴瘤患者中捕捉到乳腺、胰腺等结外受累信号。这些变化与患者临床信息所揭示的器官受累趋势总体一致,提示该技术在早期预警和系统评估中的潜力。需要说明的是,部分队列因缺乏影像学对照,其信号变化与真实器官受累的相关性仍有待进一步验证。
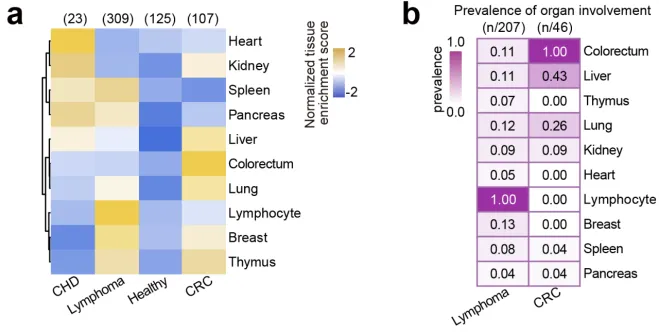
无偏溯源结果与临床表型比较
与传统液体活检往往局限于单病种或单一靶标的“点状”检测不同,cf-EpiTracing成功实现了从“靶点检测”向“系统状态评估”的范式跨越。这一基于染色质表观调控特征的无偏解析框架,视野更为宏大,为复杂疾病的无创精准诊断筑牢了稳定、可扩展的技术基石。
全过程描绘病变的“演化轨迹”——“预防”与“善后”并行,助力导航精准医疗
在结直肠癌早诊早筛领域,cf-EpiTracing交出了一份亮眼的成绩单。通过整合游离染色质上多模态表观组学特征并结合机器学习算法,cf-EpiTracing可实现对结直肠癌与健康人群的高精度区分。模型在训练队列中准确率高达97.6%,即便在独立验证队列中,准确率仍稳居92.2%,展现出了极佳的稳健性。
在癌前病变阶段,cf-EpiTracing同样表现出良好的识别能力,对结直肠腺瘤的检出率达到77.3%,为疾病前移干预提供了有力工具。同时,该技术能够精准区分结肠癌与直肠癌不同亚型,在早期患者(I期66.7%,II期69.2%)及进展期患者(III期80.0%,IV 期100.0%)中均保持较高分型准确率,凸显了其在疾病全周期管理中的应用潜力。
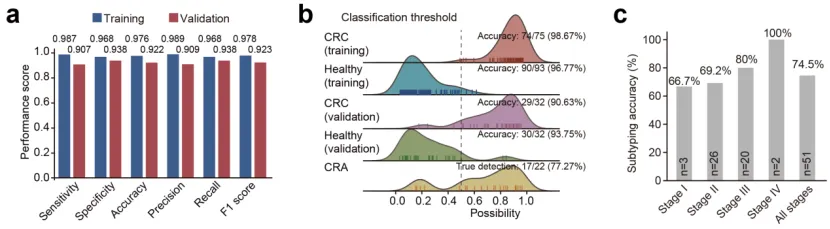
结直肠癌/腺瘤诊断及亚型分型表现
在B细胞淋巴瘤研究中,cf-EpiTracing进一步展现出解析疾病分型与演变轨迹的能力。基于细胞类型特异性的染色质状态特征,该技术能够区分不同细胞起源的淋巴瘤亚型,并在纵向样本中捕捉疾病从低侵袭性(滤泡淋巴瘤,预后较好)向高侵袭性(弥漫大B细胞淋巴瘤,预后较差)亚型转化过程中连续的表观遗传变化。同时,结合cfDNA染色质的表观信号可以提高外周血检测套细胞淋巴瘤染色体异位t(11:14)的能力。
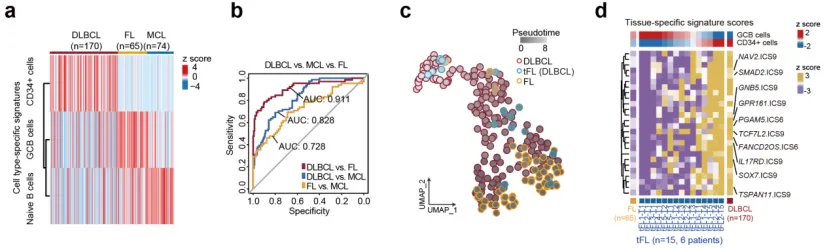
B细胞淋巴瘤亚型分型与亚型转换追踪
在治疗响应与预后评估方面,cf-EpiTracing 同样能够提供预判。研究团队构建的复发风险预测模型,展现出了超越现有临床评分体系的识别能力,成功将高、低风险患者精准分流。这表明,表观遗传信息已确立为独立于传统病理分期之外的新标尺。通过对多模态表观调控的深度解析,cf-EpiTracing 打破了“只看当下”的局限。它既能映射疾病现状,更能前瞻性地预演未来进展,为临床医生制定个体化治疗方案提供了极具价值的分子导航。
未来,cf-EpiTracing将沿“技术迭代—临床验证—产业转化”路径持续推进,加快试剂盒研发与合规化落地。团队计划开展覆盖数十种高发疾病、数十万例样本的多中心研究,重点突破胰腺癌、脑部肿瘤、前列腺癌及神经系统疾病的早诊瓶颈。
北京大学未来技术学院博士生陈旭斌,北京大学—清华大学生命科学联合中心博士生孟晓萱,北京大学第三医院血液科张伟龙博士,以及中国人民解放军总医院第五医学中心博士生张夏玮为论文共同第一作者。北京大学未来技术学院、北京大学—清华大学生命科学联合中心、北京大学成都前沿交叉生物技术研究院和北京大学肿瘤医院何爱彬教授,北京大学第三医院血液科景红梅主任,中国人民解放军总医院血液病医学部窦立萍主任,以及上海交通大学医学院郑俊克教授为本文通讯作者。阜外医院周洲主任和周维真老师在技术早期探索与优化阶段给予了样本支持。该研究获得了国家重点基础研究发展计划、教育部基础与交叉学科突破计划、国家自然科学基金委和生命科学联合中心的支持。

